מְחַבֵּר:
Eric Farmer
תאריך הבריאה:
10 מרץ 2021
תאריך עדכון:
1 יולי 2024

תוֹכֶן
- צעדים
- שיטה 1 מתוך 2: קביעת מספר הנויטרונים באטומים (לא איזוטופים)
- שיטה 2 מתוך 2: קביעת מספר הניוטרונים באיזוטופים
- טיפים
באטומים של אותו יסוד מספר הפרוטונים קבוע, בעוד מספר הנויטרונים יכול להשתנות.על ידי ידיעה כמה נויטרונים יש באטום מסוים, אתה יכול לקבוע אם זהו אטום רגיל או איזוטופ שיהיו בו פחות או יותר נויטרונים. קביעת מספר הנויטרונים באטום היא פשוטה למדי. כל מה שאתה צריך לעשות כדי לחשב את מספר הנויטרונים באטום או באיזוטופ הוא לעקוב אחר ההנחיות שלנו ולשמור על הטבלה המחזורית בהישג יד.
צעדים
שיטה 1 מתוך 2: קביעת מספר הנויטרונים באטומים (לא איזוטופים)
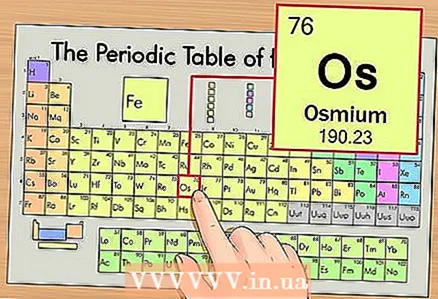 1 מצא את האלמנט בטבלה המחזורית. כדוגמה, נשקול אוסמיום (Os), שנמצא בתקופה השישית (שורה שישית מלמעלה).
1 מצא את האלמנט בטבלה המחזורית. כדוגמה, נשקול אוסמיום (Os), שנמצא בתקופה השישית (שורה שישית מלמעלה).  2 מצא את המספר האטומי של היסוד. זהו, ככלל, המספר הבולט ביותר בתא של יסוד והוא ממוקם בדרך כלל מעל הסמל שלו (בגרסת הטבלה המחזורית בה אנו משתמשים בדוגמה שלנו, אין מספרים אחרים). המספר האטומי הוא מספר הפרוטונים באטום אחד של אותו יסוד. עבור אוסמיום, מספר זה הוא 76, כלומר, ישנם 76 פרוטונים באטום אוסמיום אחד.
2 מצא את המספר האטומי של היסוד. זהו, ככלל, המספר הבולט ביותר בתא של יסוד והוא ממוקם בדרך כלל מעל הסמל שלו (בגרסת הטבלה המחזורית בה אנו משתמשים בדוגמה שלנו, אין מספרים אחרים). המספר האטומי הוא מספר הפרוטונים באטום אחד של אותו יסוד. עבור אוסמיום, מספר זה הוא 76, כלומר, ישנם 76 פרוטונים באטום אוסמיום אחד. - מספר הפרוטונים אינו משתנה, וזה מה שהופך אלמנט ליסוד.
 3 מצא את המסה האטומית של יסוד. מספר זה נמצא בדרך כלל מתחת לסמל האלמנט. שים לב שבגרסת הטבלה המחזורית בדוגמה שלנו, המסה האטומית אינה ניתנת (לא תמיד זה המצב; בהרבה גרסאות של הטבלה המחזורית מסומנת המסה האטומית). המסה האטומית של האוסמיום היא 190.23.
3 מצא את המסה האטומית של יסוד. מספר זה נמצא בדרך כלל מתחת לסמל האלמנט. שים לב שבגרסת הטבלה המחזורית בדוגמה שלנו, המסה האטומית אינה ניתנת (לא תמיד זה המצב; בהרבה גרסאות של הטבלה המחזורית מסומנת המסה האטומית). המסה האטומית של האוסמיום היא 190.23.  4 עיגול המסה האטומית למספר השלם הקרוב ביותר. בדוגמה שלנו, 190.23 מעוגל ל -190.
4 עיגול המסה האטומית למספר השלם הקרוב ביותר. בדוגמה שלנו, 190.23 מעוגל ל -190. - המסה האטומית היא המספר הממוצע של איזוטופים של יסוד מסוים, בדרך כלל הוא אינו מתבטא כמספר שלם.
 5 הפחת את המספר האטומי מהמסה האטומית. מכיוון שהפרוטונים והנויטרונים מהווים את החלק המוחלט של המסה האטומית, חיסור מספר הפרוטונים (כלומר המספר האטומי, השווה למספר הפרוטונים) מהמסה האטומית נותן את מספר הנויטרונים באטום. המספרים אחרי הנקודה העשרונית מתייחסים למסה הקטנה מאוד של האלקטרונים באטום. בדוגמה שלנו: 190 (משקל אטומי) - 76 (מספר פרוטונים) = 114 (מספר נויטרונים).
5 הפחת את המספר האטומי מהמסה האטומית. מכיוון שהפרוטונים והנויטרונים מהווים את החלק המוחלט של המסה האטומית, חיסור מספר הפרוטונים (כלומר המספר האטומי, השווה למספר הפרוטונים) מהמסה האטומית נותן את מספר הנויטרונים באטום. המספרים אחרי הנקודה העשרונית מתייחסים למסה הקטנה מאוד של האלקטרונים באטום. בדוגמה שלנו: 190 (משקל אטומי) - 76 (מספר פרוטונים) = 114 (מספר נויטרונים). 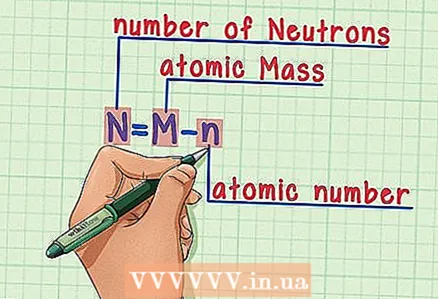 6 זכור את הנוסחה. כדי למצוא את מספר הנויטרונים בעתיד, פשוט השתמש בנוסחה הבאה:
6 זכור את הנוסחה. כדי למצוא את מספר הנויטרונים בעתיד, פשוט השתמש בנוסחה הבאה: - N = M - n
- N = מספר הנויטרונים
- M = מסה אטומית
- n = מספר אטומי
- N = M - n
שיטה 2 מתוך 2: קביעת מספר הניוטרונים באיזוטופים
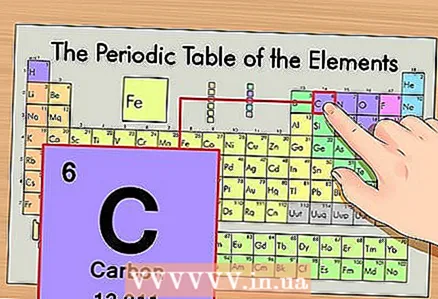 1 מצא את האלמנט בטבלה המחזורית. כדוגמה, נשקול את האיזוטופ של פחמן 14C. מכיוון שהפחמן הלא-איזוטופי 14C הוא רק פחמן C, מצא פחמן בטבלה המחזורית (תקופה שנייה או שורה שנייה מלמעלה).
1 מצא את האלמנט בטבלה המחזורית. כדוגמה, נשקול את האיזוטופ של פחמן 14C. מכיוון שהפחמן הלא-איזוטופי 14C הוא רק פחמן C, מצא פחמן בטבלה המחזורית (תקופה שנייה או שורה שנייה מלמעלה). 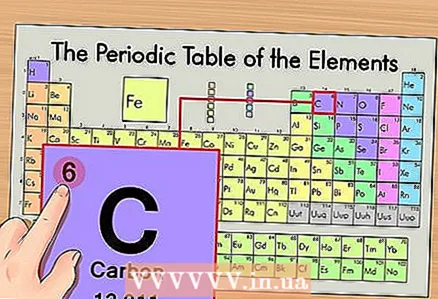 2 מצא את המספר האטומי של היסוד. זהו, ככלל, המספר הבולט ביותר בתא של יסוד והוא ממוקם בדרך כלל מעל הסמל שלו (בגרסת הטבלה המחזורית בה אנו משתמשים בדוגמה שלנו, אין מספרים אחרים). המספר האטומי הוא מספר הפרוטונים באטום אחד של אותו יסוד. פחמן הוא מספר 6, כלומר לפחמן אחד יש שישה פרוטונים.
2 מצא את המספר האטומי של היסוד. זהו, ככלל, המספר הבולט ביותר בתא של יסוד והוא ממוקם בדרך כלל מעל הסמל שלו (בגרסת הטבלה המחזורית בה אנו משתמשים בדוגמה שלנו, אין מספרים אחרים). המספר האטומי הוא מספר הפרוטונים באטום אחד של אותו יסוד. פחמן הוא מספר 6, כלומר לפחמן אחד יש שישה פרוטונים. 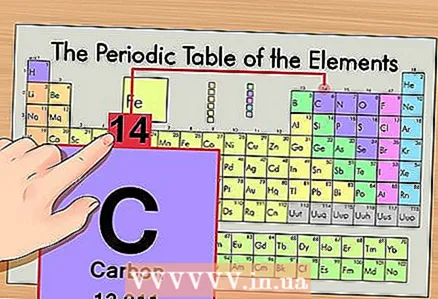 3 מצא את המסה האטומית. במקרה של איזוטופים, קל מאוד לעשות זאת, מכיוון שהם נקראים על פי המסה האטומית שלהם. במקרה שלנו, לפחמן 14C יש מסה אטומית של 14. כעת אנו יודעים את המסה האטומית של האיזוטופ; תהליך החישוב שלאחר מכן הוא זהה לקביעת מספר הנויטרונים באטומים (לא איזוטופים).
3 מצא את המסה האטומית. במקרה של איזוטופים, קל מאוד לעשות זאת, מכיוון שהם נקראים על פי המסה האטומית שלהם. במקרה שלנו, לפחמן 14C יש מסה אטומית של 14. כעת אנו יודעים את המסה האטומית של האיזוטופ; תהליך החישוב שלאחר מכן הוא זהה לקביעת מספר הנויטרונים באטומים (לא איזוטופים).  4 הפחת את המספר האטומי מהמסה האטומית. מכיוון שהפרוטונים והנויטרונים מהווים את החלק המוחלט של המסה האטומית, חיסור מספר הפרוטונים (כלומר המספר האטומי, השווה למספר הפרוטונים) מהמסה האטומית נותן את מספר הנויטרונים באטום. בדוגמה שלנו: 14 (מסת אטומית) - 6 (מספר פרוטונים) = 8 (מספר נויטרונים).
4 הפחת את המספר האטומי מהמסה האטומית. מכיוון שהפרוטונים והנויטרונים מהווים את החלק המוחלט של המסה האטומית, חיסור מספר הפרוטונים (כלומר המספר האטומי, השווה למספר הפרוטונים) מהמסה האטומית נותן את מספר הנויטרונים באטום. בדוגמה שלנו: 14 (מסת אטומית) - 6 (מספר פרוטונים) = 8 (מספר נויטרונים). 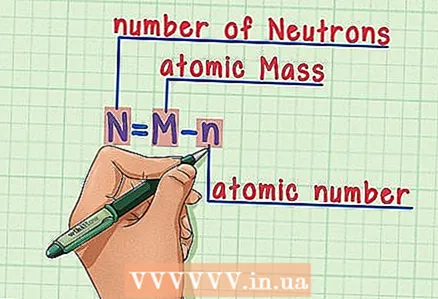 5 זכור את הנוסחה. כדי למצוא את מספר הנויטרונים בעתיד, פשוט השתמש בנוסחה הבאה:
5 זכור את הנוסחה. כדי למצוא את מספר הנויטרונים בעתיד, פשוט השתמש בנוסחה הבאה: - N = M - n
- N = מספר הנויטרונים
- M = מסה אטומית
- n = מספר אטומי
- N = M - n
טיפים
- פרוטונים ונויטרונים מהווים כמעט את המסה המוחלטת של היסודות, בעוד שאלקטרונים וחלקיקים אחרים מהווים מסה לא משמעותית ביותר (המסה הזו נוטה לאפס).מכיוון שלפרוטון אחד יש אותה מסה של נויטרון אחד, והמספר האטומי הוא מספר הפרוטונים, אתה יכול פשוט להפחית את מספר הפרוטונים מהמסה הכוללת.
- אוסמיום - מתכת במצב מוצק בטמפרטורת החדר, קיבלה את שמה מהמילה היוונית "אוסמה" - ריח.
- אם אינך בטוח מה פירוש מספר בטבלה המחזורית, זכור: הטבלה בנויה בדרך כלל סביב מספר אטומי (כלומר מספר הפרוטונים), המתחיל ב -1 (מימן) וגדל יחידה אחת משמאל לימין , שמסתיים ב- 118 (Oganesson). הסיבה לכך היא שמספר הפרוטונים באטום קובע את היסוד עצמו, ומספר כזה הוא הדרך הקלה ביותר לארגן את היסודות (לדוגמה, אטום בעל 2 פרוטונים הוא תמיד הליום, בדיוק כמו שאטום עם 79 פרוטונים הוא תמיד זהב ).