מְחַבֵּר:
Monica Porter
תאריך הבריאה:
17 מרץ 2021
תאריך עדכון:
1 יולי 2024

תוֹכֶן
ריכוז טוחנת מציין את הקשר בין מספר השומות של מומס לנפח התמיסה. כדי לחשב טוחנות, אתה יכול להתחיל עם שומות ונפח, מסה ונפח, או שומות ומיליליטר (מ"ל). לאחר מכן, עם המשתנים לעיל, החל את הנוסחה הבסיסית של ריכוז טוחנת כדי לקבל את התוצאה הנכונה.
צעדים
שיטה 1 מתוך 4: חישוב ריכוז מול ממספר הטוחנת והנפח
חשוב לדעת את הנוסחה הבסיסית לחישוב הריכוז הטוחנת. ריכוז טוחנת השווה למספר השומות של מומס חלקי נפח התמיסה בליטר. משם יש לנו את הנוסחה הבאה: ריכוז טוחנת = מספר שומות מומס / מספר ליטר תמיסה
- דוגמה: מהו הריכוז הטוחני של תמיסה המכילה 0.75 שומן NaCl ב -4.2 ליטר תמיסה?

ניתוח הנושא. כדי לחשב את הריכוז הטוחני, אתה צריך את מספר השומות ואת נפח התמיסה בליטר. אינך צריך לחשב את שני הערכים הללו בגלל הנושא הנתון.- לדוגמה:
- מספר השומות = 0.75 שומות NaCl
- נפח = 4.2 ליטר
- לדוגמה:
חלק את מספר השומות בנפח. התוצאה של חלוקת השומה לפי נפח היא מספר השומות לליטר תמיסה, או הריכוז הטוחני של התמיסה.
- דוגמה: ריכוז טוחנת = מספר שומות מומס / מספר ליטר תמיסה = 0.75 מול / 4.2 ליטר = 0.17857142

רשום את התוצאות שלך. עגול לשניים-שלושה מספרים אחרי פסיק, תלוי בבקשת המורה או במשימה. בעת רישום התוצאות שלך, קיצור "ריכוז טוחנת" ב- "M" והוסף את הסמל הכימי של המומס.- לדוגמה: 0.179 מ 'NaCl
שיטה 2 מתוך 4: חישוב ריכוז מול ממסה ונפח
יש לדעת את הנוסחה הבסיסית לחישוב הריכוז הטוחנת. ריכוז טוחנת מראה את הקשר בין מספר השומות של מומס לנפח התמיסה. הנוסחה לריכוז הטוחנת היא כדלקמן: ריכוז טוחנת = ריכוז מומס / מספר ליטר תמיסה
- דוגמא לבעיה: חשב את מספר השומות של התמיסה עם המסת 3.4 גרם KMnO4 ב -5.2 ליטר מים.

ניתוח הנושא: כדי למצוא את הריכוז הטוחני, אתה צריך את מספר השומות ואת נפח התמיסה בליטר. אם ערכים אלה לא ניתנים, אך אתה יודע את נפח המסה והמיסה של התמיסה, אתה יכול לקבוע את מספר שומות המומס לפני חישוב הריכוז הטוחני.- לדוגמה:
- משקל = 3.4 גרם KMnO4
- נפח = 5.2 ליטר
- לדוגמה:
חשב את מולקולת המסה של המומס. כדי לחשב את מספר שומות המומס מאותה המסה או גרם המומס, ראשית עליך לקבוע את מולקולת המסה של המומס. ניתן לקבוע את מולקולת המסה של מומס על ידי הוספת אטום המסה של כל יסוד בתמיסה. כדי למצוא את האטום המעוקב של כל יסוד, השתמש בטבלה המחזורית של היסודות.
- לדוגמה:
- אטום מסה של K = 39.1 גרם
- אטום מסה של Mn = 54,9 גרם
- אטום מסה של O = 16,0 גרם
- סה"כ אטומי מסה = K + Mn + O + O + O + O = 39.1 + 54.9 + 16 + 16 + 16 + 16 = 158.0 גרם
- לדוגמה:
להמיר גרם לשומות. ברגע שיש לך מולקולה מעוקבת, עליך להכפיל את מספר גרם המומס בתמיסה במקדם ההמרה המקביל של 1 מול למסה מולרית של המומס. התוצאה של הכפל זה היא מספר השומות של המומס.
- דוגמה: גרם מומס * (1 / מסה מולרית של מומס) = 3.4 גרם * (1 מול / 158 גרם) = 0.0215 מול
חלק את מספר השומות במספר ליטרים. כעת, לאחר שחישבתם את מספר השומות, כעת חלקו את המספר בנפח התמיסה בליטר, יהיה לכם הריכוז הטוחני של התמיסה ההיא.
- דוגמה: ריכוז טוחנת = מספר שומות מומס / מספר ליטרים של תמיסה = 0.0215 mol / 5.2 L = 0.004134615
רשום את התוצאות שלך. עליך לעגל את התוצאות כנדרש על ידי המורה, בדרך כלל שניים עד שלושה מספרים אחרי פסיק. בנוסף, בעת כתיבת התוצאה יש לקצר את "ריכוז הטוחנת" ל "M" וללוות את הסמל הכימי של המומס.
- לדוגמה: 0.004 מ 'KMnO4
שיטה 3 מתוך 4: חישב את ריכוז הטוחנת ממספר השומות והמיליליטר של התמיסה
צריך לדעת את הנוסחה לריכוז הטוחנת. לחישוב הריכוז הטוחני. עליכם לחשב את מספר השומות של המומס לליטר תמיסה, ולא את מיליליטר התמיסה. הנוסחה הכללית לחישוב הריכוז הטוחנת היא: ריכוז טוחנת = מספר שומות מומס / מספר ליטר תמיסה
- דוגמא: חשב את הריכוז הטוחני של תמיסה המכילה 1.2 שומן CaCl2 ב- 2905 מיליליטר מים.
לנתח את הנושא. כדי לחשב את הריכוז הטוחני, אתה צריך את מספר השומות של המומס ואת נפח התמיסה בליטר. אם נפח התמיסה ניתן בבעיה במיליליטר, המירו לנפח המקביל בליטר לפני ביצוע החישוב.
- לדוגמה:
- מספר השומות = 1.2 שומות של CaCl2
- נפח = 2905 מ"ל
- לדוגמה:
להמיר מיליליטר לליטר. כדי להמיר את התמיסה ממיליליטר לליטר, חלק את מספר המיליליטר ב -1000, מכיוון שכל ליטר שווה ל -1000 מיליליטר. ניתן גם להמיר מיליליטר לליטר על ידי הזזת הנקודה העשרונית 3 ספרות שמאלה.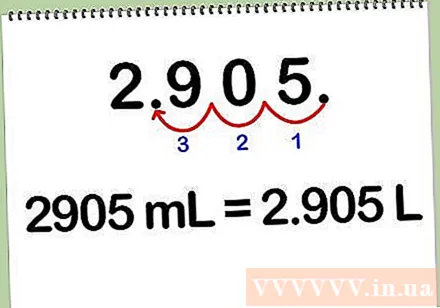
- לדוגמא: 2905 מ"ל * (1 ליטר / 1000 מ"ל) = 2,905 ליטר
חלק את מספר השומות במספר ליטרים. לאחר שיש לך מספר ליטרים, אתה יכול לחשב את ריכוז הטוחנת על ידי חלוקת מספר השומות במספר ליטר התמיסה.
- דוגמא: ריכוז טוחנת = מספר שומות מומס / מספר ליטרים של תמיסה = 1.2 שומן CaCl2 / 2,905 ל = 0.413080895
רשום את התוצאות שלך. זכור לעגל את התוצאה לשתיים או שלוש פסיקים, או לפי בקשת המורה שלך. בעת רישום התוצאה, יש לקצר את "ריכוז הטוחנת" כ- "M" ואז את הסמל הכימי של המומס.
- לדוגמה: 0.413 מ 'CaCl2
שיטה 4 מתוך 4: תרגול נוסף
חשב את הריכוז הטוחני של תמיסה כאשר 5.2 גרם NaCl מומס ב 800 מ"ל מים. קבע את הערכים הניתנים על ידי הבעיה: מסה בגרמים ונפח במיליליטר.
- מסה = 5.2 גרם NaCl
- נפח = 800 מ"ל מים
מצא את מולקולת המסה של NaCl על ידי הוספת האטום הקובי של יסוד Na, ואת האטום הקובי של Cl.
- אטום מסה של Na = 22.99 גרם
- אטום מסה של Cl = 35.45 גרם
- מולקולות מסה של NaCl = 22.99 + 35.45 = 58.44 גרם
הכפל את מסת המומס בגורם ההמרה הטוחנת. בדוגמה זו, המסה המולקולרית של NaCl היא 58.44 גרם, ולכן מקדם ההמרה הוא "1 מול / 58.44 גרם".
- מספר שומה NaCl = 5.2 גרם NaCl * (1 mol / 58.44 גרם) = 0.8898 mol = 0.09 mol
חלקו 800 מ"ל מים ב- 1000, תקבלו את נפח המים בליטר.
- ניתן גם להכפיל 800 מ"ל בגורם ההמרה 1 ליטר / 1000 מ"ל ממיליליטר לליטר.
- כדי לקצר את תהליך הכפל כנ"ל, אתה יכול לחזור את הנקודה העשרונית 3 ספרות שמאלה.
- נפח = 800 מ"ל * (1 ליטר / 1000 מ"ל) = 800 מ"ל / 1000 מ"ל = 0.8 ליטר
חלק את מספר שומות המומס בנפח התמיסה בליטר. כדי לחשב את הריכוז הטוחני, עליך לחלק 0.09 שומות של מומס (במקרה זה, NaCl) בנפח התמיסה בליטר.
- ריכוז טוחנת = מספר שומות מומס / מספר ליטר תמיסה = 0.09 mol / 0.8 L = 0.1125 mol / L
רשום את התוצאה הסופית. לעגל את התוצאה לשניים-שלושה מספרים אחרי הפסיק ולקצר את "ריכוז הטוחנת" עם "M" יחד עם הסמל הכימי המומס.
- תוֹצָאָה: 0.11 מ 'NaCl