מְחַבֵּר:
Lewis Jackson
תאריך הבריאה:
5 מאי 2021
תאריך עדכון:
1 יולי 2024

תוֹכֶן
מול היא יחידת המידה הסטנדרטית בכימיה, המשמשת לבדיקת היסודות השונים בתרכובת. בדרך כלל מסת תרכובת מחושבת בגרם (גרם) ויש להמיר אותה ליחידות טוחנות. המעבר הוא די פשוט, עם זאת, ישנם עדיין כמה צעדים חשובים שעלינו לבצע. בעזרת השיטה שלהלן תוכלו להמיר גרם בקלות לשומות.
צעדים
חלק 1 מתוך 2: חישוב המסה המולקולרית
הכן את האספקה הדרושה כדי לפתור את בעיית המתמטיקה. כשיש לך את כל הכלים הזמינים, יהיה קל יותר לפתור את הבעיה. מה שאתה צריך זה:
- עיפרון ונייר. המתמטיקה נעשית קלה יותר כשכותבים הכל על נייר. עליכם להציג את כל השלבים על מנת להגיע לציון המקסימלי.
- טבלה מחזורית של יסודות כימיים: משמשת לקביעת אטומי המסה של היסודות.
- מחשבון כיס: משמש לחישוב מספרים מסובכים.

קבע אילו אלמנטים נמצאים במתחם שעליך להמיר ליחידות טוחנות. השלב הראשון בחישוב המסה המולקולרית הוא קביעת היסודות המרכיבים את התרכובת. זה קל מכיוון שהקיצור לאלמנטים הוא רק תו עד שניים.- אם חומר מקוצר בשתי תווים, האות הראשונה באותיות רישיות והאות השנייה באותיות קטנות. דוגמה: Mg הוא הקיצור של היסוד מגנזיום.
- תרכובות NaHCO3 מורכב מארבעה יסודות: נתרן (Na), מימן (H), פחמן (C) וחמצן (O).
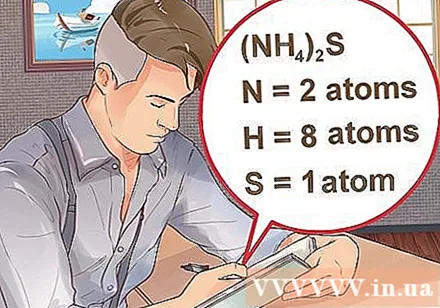
קבע את מספר האטומים עבור כל יסוד בתרכובת. עליכם לדעת את המספר האטומי של כל חומר בתרכובת כדי לחשב את מולקולת המסה של אותה תרכובת. המספר הקטן ליד קיצור היסוד מייצג את מספר האטום של היסוד.- דוגמה: תרכובת H2ל- O שני אטומי מימן ואטום חמצן אחד.
- אם תרכובת נכתבת בסוגריים, מלווה באינדקס קטן, המשמעות היא שכל מרכיב בסוגריים מכפיל את האינדקס. דוגמה: מתחם (NH4)2S מורכב משני אטומי N, שמונה אטומי H ואטום S אחד.

כתוב את הנייר האטומי הקובי עבור כל יסוד. השימוש בטבלה המחזורית היא הדרך הקלה ביותר למצוא את האטום הקובי של יסוד. לאחר שתאתר את היסוד בטבלה המחזורית, תראה את המסה האטומית ממש מתחת לסמל היסוד.- לדוגמה, האטום המעוקב של חמצן הוא 15.99.
חשב את המסה המולקולרית. מולקולת המסה של חומר שווה למספר האטומים של כל יסוד המוכפל באטום המסה של אותו יסוד. כמות זו חיונית בהמרה גרם לטוחנת.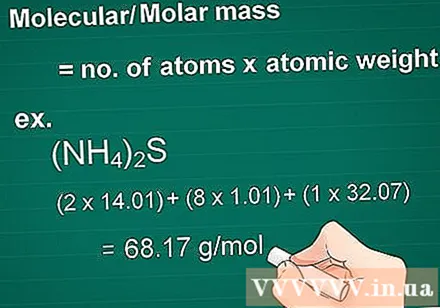
- ראשית, הכפל את המספר האטומי של כל יסוד בתרכובת באטום המסה שלו.
- לאחר מכן, הוסיפו את מסות האלמנטים במתחם יחד.
- דוגמא: מסת מולקולרית של תרכובת (NH4)2S = (2 x 14.01) + (8 x 1.01) + (1 x 32.07) = 68.17 גרם למול.
- מסת מולקולרית מכונה גם מסה טוחנת.
חלק 2 מתוך 2: המירו גרם למול
הגדר את נוסחת ההמרה. כדי למצוא את מספר השומות של התרכובת, חלק את מספר הגרמים של התרכובת במסה הטוחנת של אותה תרכובת.
- נוסחה: מספר שומות = מסה (גרם) / מסה טוחנת של תרכובת (גרם / מול)
החלף את המספרים בנוסחה. לאחר הגדרת הנוסחה הנכונה, השלב הבא הוא החלפת המספרים שחישבת לנוסחה. אם ברצונך לוודא שהנתונים נמצאים במצב הנכון, תוכל לבדוק אותם על ידי דיכוי היחידה. אם אחרי הפשטות היחידה שנותרה היא שומות אז אתה מוגדר כהלכה.
פתור את המשוואה. חלקו את המסה באמצעות מחשבון במולקולה הקובית של החומר או התרכובת. המרכיב יהיה מספר השומות של החומר או התרכובת שאתה מחפש.
- לדוגמא, הבעיה היא עבור 2 גרם מים (H2O) ובקש ממך להמיר אותו ליחידות טוחנות. יש לנו את המסה הטוחנת של H2O הוא 18 גרם למול. חלקו 2 ב- 18, כך שיהיה לכם 0.1111 mol H2O.
עֵצָה
- אל תשכח לכלול את התשובות את אלמנט או שם מורכב.
- אם תתבקש להציג את התרגיל או את החידון, הקפד להציג את התשובות שלך בצורה ברורה על ידי הקפה או ציור תיבה סביב התשובות.
מה אתה צריך
- טבלה מחזורית כימית
- עִפָּרוֹן
- עיתון
- מַחשֵׁב
- בעיות בכימיה