מְחַבֵּר:
Christy White
תאריך הבריאה:
8 מאי 2021
תאריך עדכון:
1 יולי 2024

תוֹכֶן
- לדרוך
- שיטה 1 מתוך 3: חלק ראשון: הבנת קונכיות אלקטרונים
- שיטה 2 מתוך 3: חלק שני: מציאת אלקטרונים ערכיים במתכות, למעט מתכות מעבר
- שיטה 3 מתוך 3: חלק שלישי: מציאת אלקטרוני ערכיות במתכות מעבר
- טיפים
- צרכים
אלקטרוני ערכיות מונחים בקליפה החיצונית של אלמנט. מספר אלקטרוני הערכיות באטום קובע את סוג הקשר הכימי שיכול יסוד זה יכול ליצור. הדרך הטובה ביותר לגלות את מספר אלקטרוני הערכיות היא להשתמש בטבלה המחזורית של היסודות.
לדרוך
שיטה 1 מתוך 3: חלק ראשון: הבנת קונכיות אלקטרונים
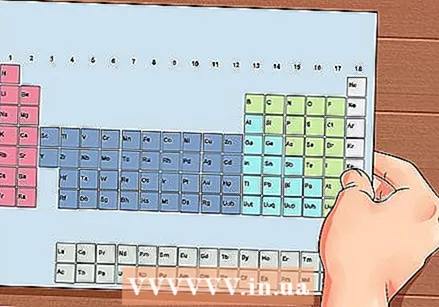 הטבלה המחזורית של האלמנטים. זוהי טבלה עם קודי צבע, כאשר בכל תא מוצג אלמנט עם המספר האטומי ו -1 עד 3 אותיות כסמל.
הטבלה המחזורית של האלמנטים. זוהי טבלה עם קודי צבע, כאשר בכל תא מוצג אלמנט עם המספר האטומי ו -1 עד 3 אותיות כסמל. 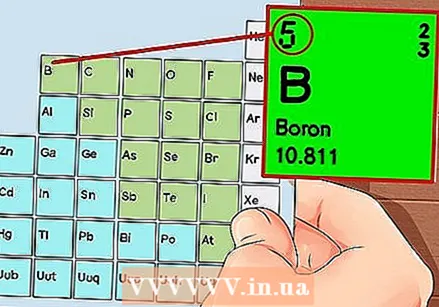 מצא את המספר האטומי של היסוד. המספר האטומי נמצא מעל או ליד סמל היסוד. לדוגמא: לבורון (B) יש מספר אטומי של 5, כלומר יש לו 5 פרוטונים ו- 5 אלקטרונים.
מצא את המספר האטומי של היסוד. המספר האטומי נמצא מעל או ליד סמל היסוד. לדוגמא: לבורון (B) יש מספר אטומי של 5, כלומר יש לו 5 פרוטונים ו- 5 אלקטרונים. 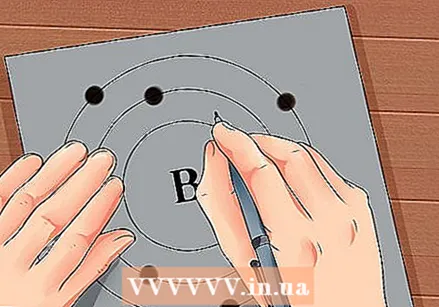 שרטטו ייצוג פשוט של אטום והניחו את האלקטרונים במסלול סביב הגרעין. עבודות אלה נקראות גם פגזים או רמות אנרגיה. המספר המרבי של אלקטרונים שיכולים להיות באותה קליפה קבוע, והקליפות מתמלאות מהמסלול הפנימי לחוץ.
שרטטו ייצוג פשוט של אטום והניחו את האלקטרונים במסלול סביב הגרעין. עבודות אלה נקראות גם פגזים או רמות אנרגיה. המספר המרבי של אלקטרונים שיכולים להיות באותה קליפה קבוע, והקליפות מתמלאות מהמסלול הפנימי לחוץ. - מעטפת K (פנימית): מקסימום 2 אלקטרונים.
- מעטפת L: מקסימום 8 אלקטרונים.
- מעטפת M: 18 אלקטרונים לכל היותר.
- מעטפת N: מקסימום 32 אלקטרונים.
- מעטפת: מקסימום 50 אלקטרונים.
- מעטפת P (חיצונית): 72 אלקטרונים לכל היותר.
 מצא את מספר האלקטרונים בקליפה החיצונית. אלה הם אלקטרוני הערכיות.
מצא את מספר האלקטרונים בקליפה החיצונית. אלה הם אלקטרוני הערכיות. - כאשר מעטפת הערכיות מלאה, האלמנט יציב.
- אם מעטפת הערכיות אינה מלאה אז היסוד הוא תגובתי, מה שאומר שהוא יכול להיקשר כימית עם האטום של יסוד אחר. כל אטום חולק את אלקטרוני הערכיות שלו בניסיון למלא את מעטפת הערכיות.
שיטה 2 מתוך 3: חלק שני: מציאת אלקטרונים ערכיים במתכות, למעט מתכות מעבר
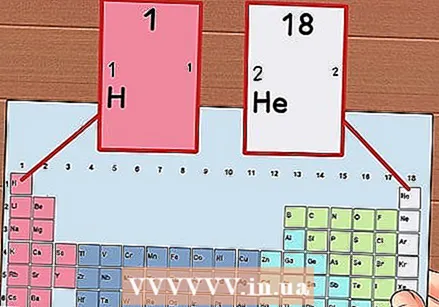 מספר כל עמודה בטבלה המחזורית, בין 1 ל -18. מימן (H) נמצא בראש עמודה 1 והליום (He) בראש עמודה 18. אלה קבוצות היסודות השונות.
מספר כל עמודה בטבלה המחזורית, בין 1 ל -18. מימן (H) נמצא בראש עמודה 1 והליום (He) בראש עמודה 18. אלה קבוצות היסודות השונות. 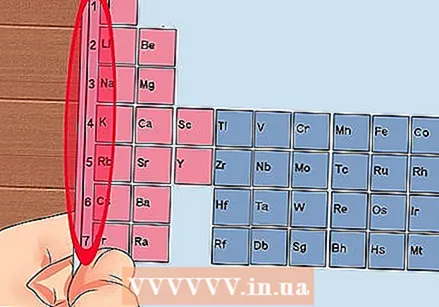 תן לכל שורה מספר, בין 1 ל -7. אלה תקופות היסודות, והם תואמים את מספר הקליפות או רמות האנרגיה של אטום.
תן לכל שורה מספר, בין 1 ל -7. אלה תקופות היסודות, והם תואמים את מספר הקליפות או רמות האנרגיה של אטום. - למימן (H) ולהליום (He) יש מעטפת אחת, בעוד שלפרנציום (Fr) יש 7.
- הלנטנידים והאקטינידים מקובצים ומופיעים מתחת לטבלה הראשית. כל הלנטנידים שייכים לתקופה 6, קבוצה 3 וכל האקטינידים שייכים לתקופה 7, קבוצה 3.
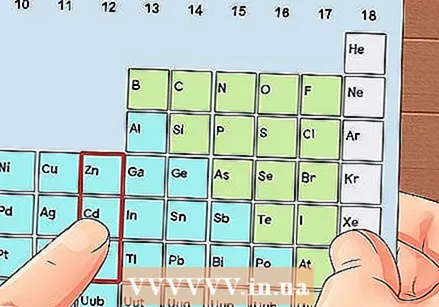 אתר אלמנט שאינו מתכת מעבר. מתכות מעבר הן בקבוצות 3 עד 12. מספר הקבוצות של המתכות האחרות מציין את מספר אלקטרוני הערכיות.
אתר אלמנט שאינו מתכת מעבר. מתכות מעבר הן בקבוצות 3 עד 12. מספר הקבוצות של המתכות האחרות מציין את מספר אלקטרוני הערכיות. - קבוצה 1: אלקטרון ערכיות
- קבוצה 2: 2 אלקטרוני ערכיות
- קבוצה 13: 3 אלקטרוני ערכיות
- קבוצה 14: 4 אלקטרוני ערכיות
- קבוצה 15: 5 אלקטרוני ערכיות
- קבוצה 16: 6 אלקטרונים ערכיים
- קבוצה 17: 7 אלקטרוני ערכיות
- קבוצה 18: 8 אלקטרוני ערכיות - למעט הליום, שיש בו 2
שיטה 3 מתוך 3: חלק שלישי: מציאת אלקטרוני ערכיות במתכות מעבר
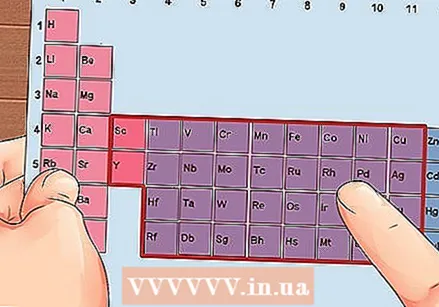 מצא אלמנט מקבוצות 3 עד 12, מתכות המעבר.
מצא אלמנט מקבוצות 3 עד 12, מתכות המעבר. קבע את מספר אלקטרוני הערכיות על סמך מספר הקבוצה. מספרים קבוצתיים אלה תואמים למספר אפשרי של אלקטרוני ערכיות.
קבע את מספר אלקטרוני הערכיות על סמך מספר הקבוצה. מספרים קבוצתיים אלה תואמים למספר אפשרי של אלקטרוני ערכיות. - קבוצה 3: 3 אלקטרוני ערכיות
- קבוצה 4: 2 עד 4 אלקטרוני ערכיות
- קבוצה 5: 2 עד 5 אלקטרוני ערכיות
- קבוצה 6: 2 עד 6 אלקטרוני ערכיות
- קבוצה 7: 2 עד 7 אלקטרוני ערכיות
- קבוצה 8: אלקטרוני ערכיות 2 או 3
- קבוצה 9: אלקטרוני ערכיות 2 או 3
- קבוצה 10: אלקטרוני ערכיות 2 או 3
- קבוצה 11: אלקטרונים ערכיים 1 או 2
- קבוצה 12: 2 אלקטרוני ערכיות
טיפים
- למתכות מעבר יכולות להיות קליפות ערכיות שאינן מלאות לחלוטין. קביעת המספר המדויק של אלקטרוני ערכיות במתכות מעבר מחייבת עקרונות מסוימים של תורת הקוונטים החורגים מתחום המאמר.
צרכים
- טבלה מחזורית של האלמנטים
- עִפָּרוֹן
- עיתון