מְחַבֵּר:
Lewis Jackson
תאריך הבריאה:
12 מאי 2021
תאריך עדכון:
1 יולי 2024

תוֹכֶן
קביעת מספר הנייטרונים באטום היא די פשוטה, אפילו לא צריך לעשות ניסויים. כדי לחשב את מספר הנויטרונים באטום או איזוטופ רגיל, אתה רק צריך להכין טבלה מחזורית ולבצע את ההוראות.
צעדים
שיטה 1 מתוך 2: מצא את מספר הנויטרונים באטום רגיל
קבע את מיקום האלמנט בטבלה המחזורית. לדוגמה, אנו נמצא את היסוד אוסמיום (Os) בשורה השישית מלמעלה.
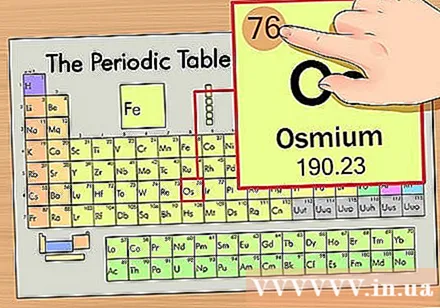
מצא את המספר האטומי של היסוד. זהו המספר הבולט ביותר שעובר על ידי כל אלמנט ונמצא מעל לסמל הראשוני (על הלוח בו אנו משתמשים אין מספרים אחרים). המספר האטומי הוא מספר הפרוטונים באטום יחיד של אותו יסוד. Os הוא המספר 76, מה שאומר שיש 76 פרוטונים באטום אוסמיום.- מספר הפרוטונים לעולם אינו משתנה באלמנט; זהו למעשה המאפיין המגדיר של אלמנט.
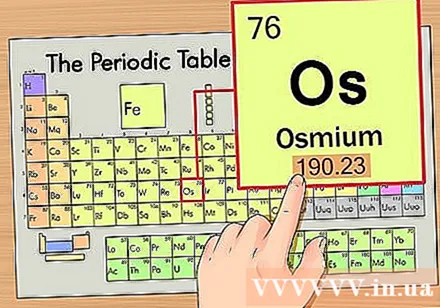
מצא את המשקל האטומי של היסוד. מספר זה נמצא בדרך כלל מתחת לסמל הראשוני. שים לב כי לטבלה המחזורית בדוגמה זו יש רק מספר אטומי וללא משקל אטומי. לא כל הטבלאות המחזוריות. לאוסמיום משקל אטומי של 190.23.
לעגל את המשקל האטומי למספר השלם הקרוב ביותר לקבלת המסה האטומית. לדוגמה, 190.23 יעגל ל -190, כך שהמסה האטומית של אוסמיום היא 190.- משקל אטומי הוא הערך הממוצע של איזוטופים של אותו יסוד כימי, ולכן זה בדרך כלל לא מספר שלם.
מחסרים את המספר האטומי ממסת האטום. מכיוון שרוב המסה האטומית היא המסה של פרוטונים ונויטרונים, חיסור מספר הפרוטונים מהמסה האטומית (כלומר, מספר אטום) לספור לקבל את מספר הנויטרונים באטום. המספר אחרי הנקודה העשרונית מייצג את המסה הקטנה ביותר של אלקטרונים באטום. בדוגמה זו יש לנו: 190 (אטום מסה) - 76 (מספר פרוטונים) = 114 (מספר נויטרונים).
שינן את המתכון. כדי למצוא את מספר הנויטרונים, אנו מיישמים את הנוסחה הבאה: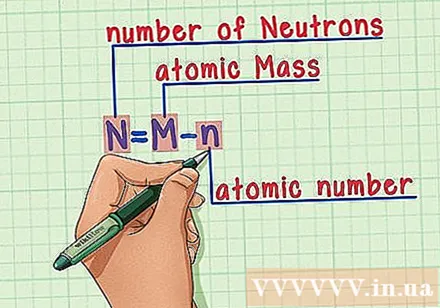
- N = M - n
- N = מספר הנויטרונים
- M = מסת אטומית
- n = מספר אטומי
- N = M - n
שיטה 2 מתוך 2: מצא את מספר הנויטרונים באיזוטופ
קבע את מיקום האלמנט בטבלה המחזורית. הבה ניקח לדוגמא את יסוד איזוטופ פחמן 14. מכיוון שצורת האיזוטופ של פחמן 14 היא פשוט פחמן (C), חפש פחמן בטבלה המחזורית (שורה שנייה מלמעלה).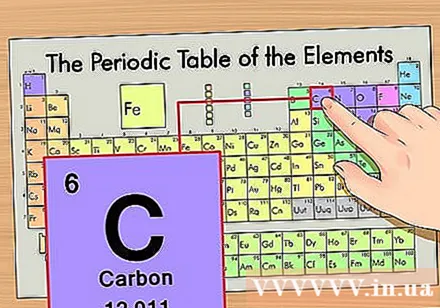
מצא את המספר האטומי של היסוד. זהו המספר הבולט ביותר שעובר על ידי כל אלמנט ונמצא מעל לסמל הראשוני (על הלוח בו אנו משתמשים אין מספרים אחרים). המספר האטומי הוא מספר הפרוטונים באטום יחיד של אותו יסוד. C הוא מספר 6, כלומר ישנם 6 פרוטונים באטום פחמן.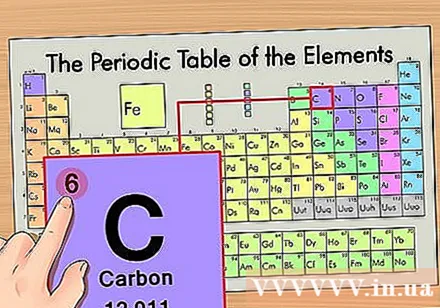
מצא מסה אטומית. זה קל מאוד עם איזוטופים מכיוון שהם נקראים על שם המסה האטומית. לדוגמא, לפחמן 14 תהיה מסה אטומית של 14. לאחר שמצאת את המסה האטומית של האיזוטופ, הצעדים הנותרים למציאת מספר הנויטרונים יהיו זהים לזה של אטום רגיל.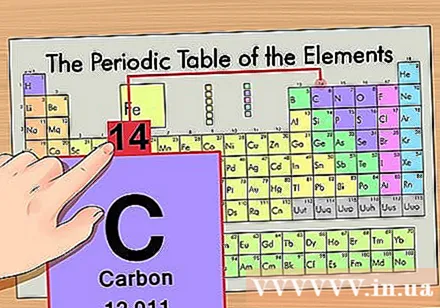
מחסרים את המספר האטומי ממסת האטום. מכיוון שרוב המסה האטומית היא המסה של פרוטונים ונויטרונים, חיסור מספר הפרוטונים מהמסה האטומית (כלומר, מספר אטום) לספור לקבל את מספר הנויטרונים באטום. המספר אחרי הנקודה העשרונית מייצג את המסה הקטנה ביותר של אלקטרונים באטום. בדוגמה זו יש לנו: 14 (אטום מסה) - 6 (מספר פרוטונים) = 8 (מספר נויטרונים).
שינן את המתכון. כדי למצוא את מספר הנויטרונים, אנו מיישמים את הנוסחה הבאה: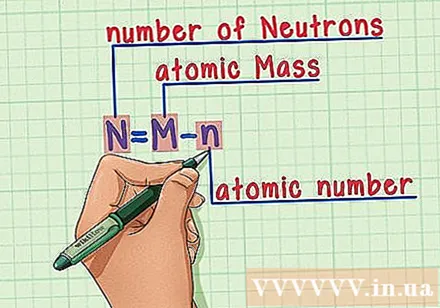
- N = M - n
- N = מספר הנויטרונים
- M = מסת אטומית
- n = מספר אטומי
- N = M - n
עֵצָה
- המסה של יסוד היא במידה רבה המסה של פרוטונים ונויטרונים, בעוד שהמונים של אלקטרונים ואלמנטים אחרים זניחים (קרוב לאפס). מכיוון שמסת הפרוטון שווה בערך למסת הנויטרון, והמספר האטומי מייצג את מספר הפרוטונים, עלינו רק לחסר את מספר הפרוטונים מהמסה הכוללת.
- אם אינך זוכר את משמעות המספרים בטבלה המחזורית, זכור כי הטבלה המחזורית בנויה בדרך כלל על מספרים אטומיים (כלומר מספר הפרוטונים), החל מ- 1 (מימן) ותוספת מילה אחת משמאל לימין, וכלה ב 118 (ununoctium). מכיוון שמספר הפרוטונים הוא מאפיין מזהה של כל אטום, זהו המאפיין הפשוט ביותר עליו מסודרים האלמנטים. (לדוגמא, אטום עם שני פרוטונים הוא תמיד הליום, כמו אטום עם 79 פרוטונים הוא תמיד זהב).
מקורות וציטוטים
- טבלה מחזורית אינטראקטיבית